材料はシリコン(Si)・ゲルマニウム(Ge)が主流です。元素周期表で見ると、炭素(C)の列に該当します。シリコンについては、砂にSiO2として含まれるので、地球上にたくさん存在します。ただ、半導体として利用する場合は、炭素の単結晶であるダイアモンドと同じ結晶構造にする必要があるため、そのまま利用することはできません。製造方法もむずかしいようです。
| 1 H 水素 |
2 He ヘリウム |
||||||||||||||||
| 3 Li リチウム |
4 Be ベリウム |
5 B ホウ素 |
6 C 炭素 |
7 N 窒素 |
8 O 酸素 |
9 F フッ素 |
10 Ne ネオン |
||||||||||
| 11 Na ナトリウ ム |
12 Mg マグネシ ウム |
13 Al アルミニ ウム |
14 Si ケイ素 |
15 P リン |
16 S 硫黄 |
17 Cl 塩素 |
18 Ar アルゴン |
||||||||||
| 19 K カリウム |
20 Ca カルシ ウム |
21 Sc スカンジ ウム |
22 Ti チタン |
23 V バナジ ウム |
24 Cr クロム |
25 Mn マンガン |
26 Fe 鉄 |
27 Co コバルト |
28 Ni ニッケル |
29 Cu 銅 |
30 Zn 亜鉛 |
31 Ga ガリウム |
32 Ge ゲルマ ニウム |
33 As ヒ素 |
34 Se セレン |
35 Br 臭素 |
36 Kr クリプトン |
シリコンの原子構造は、中央に原子核、第1軌道(K殻)に電子2個、第2軌道(L殻)に電子8個、第3軌道(M殻)に電子4個が周っています。
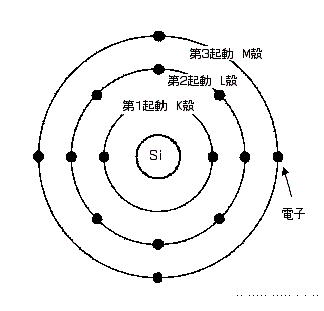
最外殻の電子を価電子といいます。
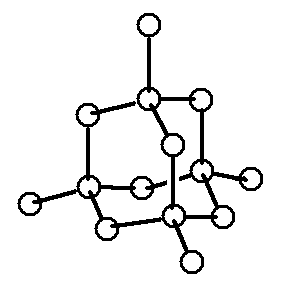
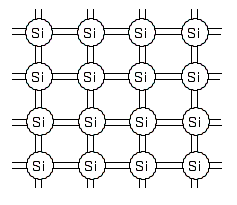
高純度のシリコン結晶は、原子どおしが4つの電子で結合し、この結合のことを共有結合といいます。シリコン結晶に自由に動ける電子はないので、電気を通しません。
N型半導体
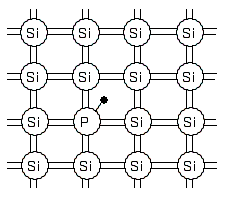
この結晶に、最外殻電子が5個の元素(例:リン)を少々混ぜます。価電子が1個余った状態になります。今度は自由に動ける電子があるので、電気の伝導性はよくなります。
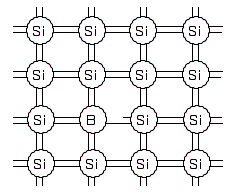
P型半導体
今度は、最外殻電子が3個の元素(例:ホウ素)を少々混ぜます。価電子が1個足りない状態になります。「正孔」といいます。この場合、正孔が自由電子のような振舞いをして、電気の伝導性はよくなります。